mTOR (포유류 라파마이신 표적) 이란?
Mammalian target of rapamycin의 약자인데, 포유류 등인 동물에서 세포 내 신호전달에 관여하는 단백질 인산화효소의 일종이다.
유기화합물인 라파마이신의 세포 내 표적단백질인데, 포유동물에 존재하는 분자량이 29만인 거대한 세린-트레어닌인산화효소이다.
진화적으로 고도로 보존되며, 일반적으로 TOR로 약칭하고 있다. mTOR은 랍터(Raptor) 등과 같이 라파마이신(rapamycin)의 표적으로서
발견하기 때문에 mTOR, 즉 포유류 라파마이신 표적 단백질의 약자로서 명명한 것이다.
라파마이신 표적 단백질인 mTOR는 식이 단백질과 아미노산을 감지하는 센서이다.
mTOR는 인슐린과 마찬가지로 성장 신호를 발신하는데, 인슐린 분비를 자극해 성장을 촉진하는 탄수화물과 마찬가지로,
mTOR를 자극해 성장을 촉진하는 단백질 섭취 역시 조절할 필요가 있다.
mTOR는 mTORC1과 mTORC2가 있다.
mTORC1은 주로 세포 성장과 대사를 조절해서 영양분에 민감하고,
mTORC2는 주로 세포 증식과 생존을 조절해서 PI3K 및 성장 인자 신호 전달을 통해 조절되는데 이러한 복합체는 뚜렷한 자극에 민감하다.
mTOR는 신체의 여러 신호 전달 경로에 참여하여 세포 증식, 자가포식 및 세포사멸을 조절한다.
정확한 메커니즘은 아직 밝혀지지 않았지만, mTOR가 너무 많으면 수명 단축, 암 및 여러 만성 건강 상태와 관련이 있으며,
너무 적으면 간 문제, 근육 위축, 치유 지연, 인슐린 민감성 장애와 같은 다른 건강 문제를 일으킬 수 있다.

근육 성장 촉진
mTOR가 활성화되면 다양한 호르몬의 활성화를 통해 근육이 성장하도록 자극한다.
근육량 감소는 노화의 첫 징후 중 하나이므로 운동을 통해 이 경로를 활성화하면 건강과 장수에 매우 유익하다.
신진대사를 증가시키는 mTOR
앞서 언급한 바와 같이, mTOR는 성장과 회복이 필요한 시기라는 신호를 신체에 보낸다.
이 신호는 ATP생성을 조절하고, 새로운 미토콘드리아를 생성하며, 신진대사를 증가시키는 방식으로 전달된다.
연구에 따르면 mTOR는 신진대사와 이화대사를 조정하는 역할과 일치하는 적절한 대사 조절에 필수적인 것으로 나타났다.
*이화작용 – 이화작용은 고분자 화합물을 저분자 유기물이나 무기물로 분해하는 과정을 말한다. 이화작용이 진행되면 에너지가 생성되어 방출된다.
이 때 방출된 에너지는 생물체가 활동하는데에 쓰이며 세포 내에서 행해지는 이화작용의 대표적인 예로는 ‘호흡’으로 볼 수 있다.
탄수화물은 소화기관을 거치면서 포도당으로 분해되고, 각 세포로 운반된다. 그 후 세포질에서 해당과정을 거쳐 피루브산으로 다시 분해되고
TCA회로에 투입되어 결국 아주 간단한 물질인 이산화탄소와 물을 만든다. 그리고 이 때 부가적으로 만들어진 물질들이 전자전달계를 거치면서
산소를 이용해 많은 양의 에너지를 낼 수 있는 ATP분자들을 만들어 낸다.
세포 내에서 일어나는 호흡뿐 아니라 소화기간에서 일어나는 소화 역시 이화작용의 한 예이다. 또 간에서는 혈당량을 일정하게 유지하기 위해
포도당과 글리코겐의 전환이 일어나는데, 혈당이 낮을 때 글리코겐을 포도당으로 분해하여 혈당을 높이는 작용 역시 이화작용이다.
동화작용이나 이화작용과 같은 물질대사는 생물체 내에서 수많은 방법으로 끊임없이 일어나고 있으며 이러한 작용이
정상적으로 진행될 때 생체가 원하는 활동을 하고 생명을 유지할 수 있는 것이다.

노화를 늦춘다
칼로리 제한에 반응하는 mTOR는 수명을 연장하고 노화 관련 질병의 발병을 늦추는 것으로 나타났다.
*인슐린 저항성이 있는 상태 만으로 근육 생성 경로들은 억제되고, 근육을 약화시키는 경로들은 활성화된다.
운동은 복잡한 경로를 통하지 않고 바로 mTOR를 활성화 한다. 또 TNF-알파로 유도되는 근단백분해를 억제하는 효과가 있다.
운동은 우리에게 부족하거나 기능저하된 인슐린과 인슐린유사성장호르몬(IGF-1)이 IRS1수용체와의 결합을 활성화하여
mTOR경로와 GLUT-4(세포내 당수송 단백질) 경로를 상향조절한다. 그 결과 근세포의 성장을 촉진하고 혈당과 인슐린 저항성을 낮추고
이는 당대사를 좋게 해주며 근육성장이 더 잘 될 수 있는 환경을 조성하는 선순환 구조를 만든다.
자폐의 새로운 원인
기초과학연구원(IBS) 시냅스 뇌질환 연구단 김은준 단장 연구팀은 TANC2 단백질 결손이 자폐 및 뇌 발달장애를 유발하는 매커니즘을 규명했다.
이로써 TANC2 유전자 돌연변이에서 기인한 자폐 및 뇌 발달장애 치료제 개발에 크게 기여할 것으로 기대된다고 하는데 좀 더 자세히 알아보자.
뇌의 발달은 세포 내 다양한 신호전달체계에 의해 조절된다. 그 중 mTOR 신호전달은 신경세포를 포함한 대부분 세포의 발달과 기능을 제어한다.
여기에는 대사 장애, 뇌 발달장애 등 다양한 질환이 관련되어있다고 알려져 있다.
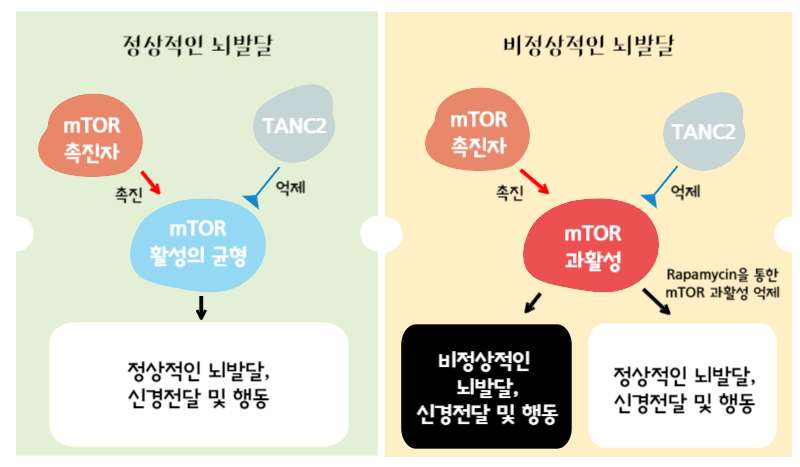
정상적인 뇌발달 상황에서 mTOR의 활성은 촉진자(Positive regulator)와 억제자(TANC2; negative regulator)에 의해 균형 있게 조절되며
정상적인 뇌발달, 신경전달 및 행동을 매개한다. 그러나, TANC2의 양이나 기능이 감소하면 그 균형이 깨져서 mTOR의 과활성화가 초래되고
비정상적인 뇌발달, 신경전달 및 행동이 유발된다는 것이다. 반면 Rapamycin과 같은 mTOR 억제 약물을 투여하면 mTOR 과활성이 억제되고
정상적인 뇌발달, 신경전달 및 행동을 회복시킬 수 있다고 한다.
연구진은 TANC2 단백질과 mTOR 신호전달의 관계를 파악하고자 TANC2 발현이 절반으로 줄어든 자폐증 생쥐모델을 제작했다.
실험 결과, TANC2 단백질 결손이 mTOR 신호전달 단백질의 비정상적 과활성화로 이어져 시냅스 및 기억/학습 등의 뇌기능이 저하되었다.
이 때 mTOR 저해 약물인 라파마이신을 투여하면 시냅스 및 뇌 인지 기능이 정상으로 회복되었다고 한다. TANC2 단백질이
mTOR 신호전달 단백질을 저해하여 뇌 기능을 조절한다는 의미이다.
나아가 인체의 신경세포에서 TANC2가 줄어들면 mTOR 신호전달체계가 비정상적으로 활성화됨도 발견했다고 한다.
인간의 신경계에서도 TANC2가 mTOR 저해인자로서 뇌 발달 및 뇌 기능을 조절하는 것이다.
* 뇌발달장애 : 자폐, 지적장애, ADHD, 뇌성마비 및 조현병 등 비정상적인 뇌발달로 인해 유발되는 다양한 뇌정신질환을 통칭함. 전세계 인구의 약 15%가 앓고 있다.
* mTOR 신호전달 : 인산화효소 단백질의 하나인 mTOR와 연관된 신호전달과정으로 세포의 사멸과 생존, 단백질 생산 등을 조절한다. 자폐 및 뇌 발달장애를 유발하는 FMRP, TSC1/2, PTEN 유전자의 돌연변이가 mTOR 신호전달 이상과 관련되어 있다.
* TANC2 단백질 : 신경세포의 흥분성 시냅스에 존재하는 단백질로 신경세포의 발달에 중요한 기능을 하는 것으로 알려져 있으며 TANC2 돌연변이와 자폐 및 뇌질환의 연관 가능성이 보고되었다.